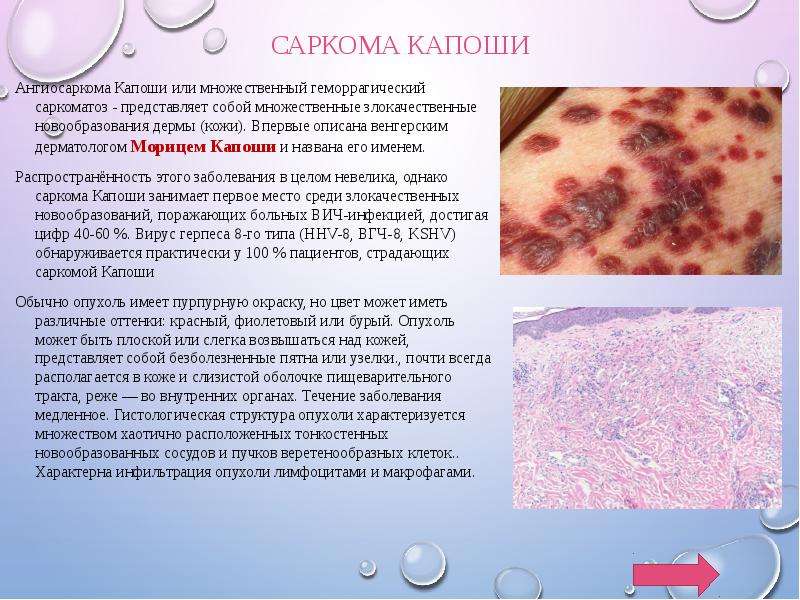
В 1872 году Мориц Капоши описал злокачественную опухоль кровеносных сосудов (первоначально она называлась «идиопатическая множественная пигментная саркома кожи»), которая также называется саркомой Капоши. Первоначально считалось, что к саркоме предрасположено еврейское и средиземноморское население, но позднее было установлено, что он широко распространен среди населения стран Африки к югу от Сахары. В 1950-х годах появились первые предположения, что эта опухоль может быть вызвана вирусом. С началом эпидемии СПИДа в начале 1980-х годов произошло внезапное увеличение зарегистрированных случаев саркомы Капоши, поражающая преимущественно больных СПИДом, причем до 50 % зарегистрированных больных СПИДом имели эту опухоль — необычайный уровень предрасположенности к раку. Тщательный анализ эпидемиологических данных, проведенных Валери Берал, Томасом Петерманом и Гарольдом Джаффе, привел этих исследователей к предположению, что причиной возникновения опухоли является неизвестный вирус, передающийся половым путем, редко вызывающий опухоли у людей с нормально функционирующей иммунной системой.
Ещё в 1984 году ученые сообщили о том, что наблюдали герпесвирусоподобные структуры в саркомах Капоши, исследованных с помощью электронной микроскопии. Ученые искали агент, вызывающий опухоль, и в качестве возможной причины было предложено более 20 агентов, включая цитомегаловирус и сам ВИЧ. В конце концов, патоген был идентифицирован в 1994 году Юаном Чангом и Патриком С. Муром, командой из его жены и мужа в Колумбийском университете, путем выделения фрагментов ДНК из герпесвируса, обнаруженного в тканях саркомы у больного СПИДом. Чанг и Мур использовали репрезентативный анализ различий, чтобы найти ГВСК, сравнивая опухолевую ткань больного СПИДом с его собственной неповрежденной тканью. Идея этого эксперимента заключалась в том, что если саркома вызывается вирусом, геномная ДНК в двух образцах должна быть точно идентичной, за исключением ДНК, принадлежащей вирусу. В своем первоначальном эксперименте они выделили два небольших фрагмента ДНК, которые составляли менее 1 % фактического вирусного генома. Эти фрагменты были похожи (но все же отличны) от известных геномов герпевирусов, что указывает на обнаружение нового вируса. Исходя из этих фрагментов, исследовательская группа смогла создать последовательность всего генома вируса менее чем через два года.
Открытие этого герпесвируса вызвало значительные споры, пока не было собрано достаточно данных, доказывающих, что ГВСК действительно является возбудителем саркомы Капоши.ГВСК представляет собой двуцепочечный ДНК-содержащий вирус. ДНК окружена икосаэдрическим капсидом, состоящим из 162 капсомеров. Снаружи вирус окружает оболочка с гликопротеиновыми шипами. Между капсидом и оболочкой расположен тегумент. После заражения вирус проникает в лимфоциты, где он остается в латентном состоянии.
Болезни, вызываемые герпесвирусом, ассоциированным с саркомой Капоши:
- Саркома Капоши
- Первичная лимфома серозных полостей
- Некоторые разновидности болезни Кастельмана
- Лимфома брюшной полости
Причина развития cаркомы Капоши (СК) – вирус герпеса человека 8 типа (HHV-8, KSHV – Kaposhi sarсoma herpes virus) относится к семейству g-herpesviridae, роду Rhadinovirus.
HHV-8 подразделяют на три варианта: А, В и С — на основании различий в нуклеотидных последовательностях субсегментов генома.
Вариант А связывают с классической СК и СПИД-ассоциированными поражениями кожи и внутренних органов.
Варианты В и С — с лимфопролиферативными заболеваниями (лимфомами, генерализованными лимфаденопатиями, болезнью Кастлемана).
Как у для других герпес-вирусов, экспрессия генов зависит стадии инфекции – латентной или литической. Во время латентной инфекции, геном HHV-8 представлен в виде эписомы и экспрессируются продукты 3 вирусных генов: ORF 72 (вирусный циклин D, угнетающий апоптоз инфицированных клеток), ORF 73 (LANA-1), и К13 (vFLIP). LANA-1 способствует распространению и транскрипции вируса в клетках за счет прикрепления ДНК HHV-8 к H1 гистону хроматина. LANA-1 угнетает транскрипционную активность р53, vFLIP защищает клетки, латентно инфицированные HHV-8 от апоптоза путем блокады Fas-рецептора и уничтожения цитотоксическими Т-лимфоцитами.
Продукт гена ORF 50 (RTA) инициирует литическую фазу жизненного цикла HHV-8. После инициации литической репликации, генные продукты производятся в упорядоченной последовательности, типичной для других герпесвирусов человека. Установлено, что до 10% вирусов HHV-8, выявляемых в очагах СК, находятся в литической фазе, однако HHV-8 в лимфоцитах периферической крови выявляется, как правило, только у больных с выраженной иммуносупрессией (СПИД-ассоциированным и иммуносупрессивным типом заболевания). Ротоглотка является местом наиболее выраженной репликации вируса; в слюне находится большое число копий вируса HHV-8.
Эпидемиология
Частота распространения классической формы саркомы Капоши (СК) значительно варьирует в различных географических областях от 0,14 на 1 млн. жителей (как мужчин, так и женщин) до 10,5 на 1 млн. мужчин и 2,7 на 1 млн. женщин. Мужчины болеют в 3 раза чаще. Начало заболевания СК регистрируется в возрасте 35-39 лет у мужчин и в возрасте 25-39 лет у женщин.
Большая частота встречаемости СК наблюдается в странах, расположенных на побережье Средиземного моря и центральной Африки (эндемическая саркома Капоши). В развитых странах у пациентов, инфицированных вирусом иммунодефицита человека (ВИЧ) –1, частота встречаемости HHV-8 наиболее высока среди мужчин гомо- и бисексуальной ориентации.
Трансплантационная СК наблюдается преимущественно при пересадке почки. Возможно развитие СК у пациентов, получающих иммуносупрессивную терапию при лечении аутоиммунных заболеваний.
Саркома Капоши является самой распространенной СПИД-ассоциированной опухолью у мужчин, практикующих сексуальные отношения с мужчинами, и наблюдается у 20% больных СПИДом.
Одним из основных путей передачи HHV-8 является половой, риск инфицирования повышается с увеличением числа сексуальных партнеров и практикой нетрадиционных видов половых контактов. Неполовой механизм передачи вируса через слюну является общепризнанным и имеет важное значение в заражении детей в эндемических областях. Вертикальный путь передачи HHV-8 от матери к плоду во время беременности и родов не имеет большого значения для распространения вируса. Вирус HHV-8 также может передаваться через кровь, продукты крови, донорские органы после трансплантаций. Вирусный геном HHV-8 обнаруживается во всех элементах СК при всех стадиях заболевания независимо от клинического варианта.
Вирус широко распространен в популяции: примерно от 1-3% доноров крови в Северной Америке до 70% в регионах Африки, где HHV-8 является эндемичным, 90% ВИЧ-инфицированных имеют антитела к литическим белкам HHV-8, сывороточные антитела к этому вирусу у здоровых доноров из России обнаруживались в 9,6% случаев.
Распространенность HHV-8 инфекции примерно отражает распространенность СК.